Гонка корпорацій: які компанії наблизились до створення вакцини від коронавірусу
Такі дані 6 липня оприлюднила Всесвітня організація охорони здоров'я. "Економічна правда" дізналася, коли чекати вакцину, які компанії наблизилися до її створення, кому вони належать, чим відрізняються їх розробки і скільки коштів вони інвестують.
Типи вакцин і стадії розробки
Вакцина - це медичний препарат біологічного походження, що провокує організм на створення імунітету до певного антигену. Вакцина зазвичай містить агент, який нагадує мікроорганізм, що викликає захворювання. Агент роблять з ослаблених або вбитих форм мікроба, його токсинів або поверхневих білків.
Для створення вакцини проти COVID-19 розробники використовують сім платформ, умовно - принципових підходів до створення вакцини.
Inactivated (інактевовані). Вакцина створюється з мікроорганізмів, вирощених в контрольованих лабораторних умовах і вбитих за допомогою термічної обробки або під впливом отрути (фенол, формалін, ацетон). Ці вакцини не здатні спричинити захворювання, але вони менш ефективні порівняно з живими вакцинами: для вироблення імунітету необхідне багаторазове введення.
Non-Replicating Viral Vector (неповторюваний віральний вектор). Вакцина створюється на базі вірусу COVID-19: з вірусу видаляють частину генів, які дозволяють відтворення (розмноження) вірусу.
RNA (РНА). ДНК-вакцина.
DNA (ДНК). Вакцина створюється шляхом вилучення з вірусу COVID-19 фрагмента ДНК (генетичного коду вірусу), монтування фрагмента в плазміду (молекулу ДНК), введення плазміди в бактерію-контейнер. Бактерія вводиться в організм, що спричиняє імунну реакцію організму. Наразі нема жодної ефективної ДНК-вакцини для людей. Є ефективні вакцини для тварин.
Protein Subunit (білкова субодиниця). Вакцина створюється з білкових або глікопротеїнових компонентів збудника, здатних спричинити захисну імунну відповідь. Виробляються за допомогою біохімічних або рекомбінантних ДНК-технологій. Такі вакцини більш ефективні, ніж живі ослаблені та інактивовані вакцини, оскільки викликають більш якісну імунологічну реакцію організму.
При цьому зникають ризики, пов'язані з поводженням із збудником. Однак субодиничні вакцини можуть бути дорожчими і можуть вимагати введення додаткових препаратів для посилення імунної відповіді.
VLP (вірусоподібні частки). Вакцина створюється на основі біологічного контейнера, який містить два білки COVID-19.
Live Attenuated Virus (живі атенуйовані вакцини). Вакцина створюється з живого вірусу, ослабленого в лабораторних умовах. Вакцина провокує імунну відповідь, яка спричиняє легку форму хвороби або не спричиняє захворювання.
На етапі клінічних випробувань найбільшу кількість вакцин розробляють на платформі ДНК і РНК. На другому місці - вакцини на платформі білкової субодиниці, потенційно це найефективніші вакцини.
Найближче до початку продажів наблизилися розробники з Китаю. Вони створюють інактевовану вакцину, яка вважається менш ефективною. Паралельно з ними йдуть розробники з Великобританії. Вони створюють вакцину на платформі "Неповторюваний віральний вектор".
|
Розробник |
Тип розробника |
Штаб-квартира |
Рік заснування |
Стадія клінічних випробувань |
Тип вакцини |
Платформа |
|
Sinovac Biotech |
приватна компанія |
Китай |
1999 |
Фаза 3 |
Inactivated + alum |
Inactivated
|
|
University of Oxford, AstraZeneca
|
університет, приватна компанія |
Великобританія, Швеція |
1996, 1913 |
Фаза 3
|
ChAdOx1-S
|
Non- Replicating Viral Vector |
|
CanSino Biological Inc., Beijing Institute of Biotechnology |
приватна компанія, університет |
Китай |
2009, 1940
|
Фаза 2 |
Adenovirus Type 5 Vector |
Non- Replicating Viral Vector |
|
Moderna, NIAID
|
приватна компанія, інститут |
США |
2010, 1955 |
Фаза 2 |
LNP- encapsulated mRNA |
RNA |
|
Inovio Pharmaceuticals, International Vaccine Institute |
приватна компанія, інститут |
США, Південна Корея |
1979, 1997 |
Фаза 1/2
|
DNA plasmid vaccine with electroporation |
DNA |
|
Cadila Healthcare Limited
|
приватна компанія |
Індія |
1952 |
Фаза 1/2 |
DNA plasmid vaccine |
DNA |
|
Wuhan Institute of Biological Products, Sinopharm |
інститут, приватна компанія
|
Китай |
1950, 2003 |
Фаза 1/2 |
Inactivated |
Inactivated |
|
Beijing Institute of Biological Products, Sinopharm |
інститут, приватна компанія |
Китай |
н. д., 2003 |
Фаза 1/2 |
Inactivated |
Inactivated |
|
Novavax |
приватна компанія |
США |
1987 |
Фаза 1/2 |
Full length recombinant SARS CoV-2 glycoprotein nanoparticle vaccine adjuvanted with Matrix M |
Protein Subunit |
|
BioNTech/Fosun Pharma, Pfizer |
приватні компанії |
Німеччина, Китай, США |
2008, 1994, 1849 |
Фаза 1/2 |
3 LNP-mRNAs |
RNA |
|
Genexine Consortium |
приватна компанія |
Південна Корея |
н. д. |
Фаза 1 |
DNA Vaccine (GX-19) |
DNA |
|
Osaka University, AnGes, Takara Bio |
університет, приватна компанія |
Японія |
1869, 1999, 2002 |
Фаза 1 |
DNA plasmid vaccine + Adjuvant |
DNA |
|
Institute of Medical Biology, Chinese Academy of Medical Sciences |
інститут |
Китай |
1956 |
Фаза 1 |
Inactivated |
Inactivated |
|
Gamaleya Research Institute
|
інститут |
Росія |
1891 |
Фаза 1 |
Adeno-based |
Non- Replicating Viral Vector |
|
Clover Biopharmaceuticals Inc., GSK/Dynavax |
приватні компанії |
Китай, США, Великобританія |
2007, 2000, 1996
|
Фаза 1
|
Native like Trimeric subunit Spike Protein vaccine |
Protein Subunit |
|
Anhui Zhifei Longcom Biopharmaceutical, Institute of Microbiology, Chinese Academy of Sciences |
приватна компанія, університет |
Китай |
н. д., 1958 |
Фаза 1 |
Adjuvanted recombinant protein (RBD- Dimer) |
Protein Subunit |
|
Vaxine Pty Ltd/Medytox
|
приватні компанії
|
Австралія, Південна Корея |
2002, 2000 |
Фаза 1 |
Recombinant spike protein with Advax™ adjuvant |
Protein Subunit |
|
Imperial College London |
інститут |
Великобританія |
1907 |
Фаза 1 |
LNP-nCoVsaRNA |
RNA |
|
Curevac |
приватна компанія |
Німеччина |
2000 |
Фаза 1 |
mRNA |
RNA |
|
People's Liberation Army (PLA) Academy of Military Sciences, Walvax Biotech |
унівиреситет, приватна компанія |
Китай |
1958, 2001 |
Фаза 1 |
mRNA |
RNA |
|
Medicago Inc., Universite Laval |
приватна компанія, університет |
Канада |
1999, 1663 |
Фаза 1 |
Plant-derived VLP |
VLP |
Стадії розробки вакцини ВООЗ класифікує за стандартами США. Це умовні чотири ключові фази, які використовує Управління із санітарного нагляду за якістю харчових продуктів і медикаментів Міністерства охорони здоров'я і соціальних служб США, більш відоме як FDA - Food and Drug Administration.
Pre-Clinical - доклінічні дослідження.
Фаза 1 - описуються результати дослідницьких випробувань, проведених перед традиційними випробуваннями, наприклад, скринінгові дослідження.
Фаза 2 - описуються результати клінічних випробувань. Розробники збирають попередні дані про те, чи діє лікарський засіб у людей, які мають певний стан чи захворювання. Тобто розробники вивчають ефективність препарату.
Фаза 3 - описуються результати клінічних випробувань. На цьому етапі збирають більше інформації про безпеку та ефективність препарату, вивчають різні групи людей, дози, застосовують препарат разом з іншими ліками. На цьому етапі в дослідженні беруть участь найбільше людей.
У випадку успішного проходження третьої фази вакцина отримує дозвіл FDA на вільний продаж на території США.
П'ять провідних розробників вакцини
Відповідно до даних ВООЗ, світовими лідерами із створення вакцини від COVID-19 є Китай. Там клінічні дослідження проводять вісім розробників. Більшість з них розробляють інактивовану вакцину.
На другому місті - США, де п'ять розробників створюють вакцину на платформі ДНК, РНК і білкової субодиниці. На третьому - Британія, де створюють вакцину на платформі неповторюваного вірального вектора, білкової субодиниці та РНК.
1. Sinovac Biotech
Китайська приватна компанія з Пекіна почала розробку вакцини від COVID-19 у січні 2020 року. Доклінічні дослідження Sinovac провела на мавпах.
Тварин імунізували однією з двох доз вакцини PiCoVacc, а потім щепили вірусом SARS-CoV-2. Тварини, які отримали найнижчу дозу вакцини, виявляли ознаки боротьби з вірусом SARS-CoV-2. Ті, які отримали найвищу дозу вакцини, виявилися більш захищеними і не мали виявлених вірусних навантажень.
Далі були проведені клінічні випробування першої та другої фаз, у яких взяли участь 743 здорові добровольці віком 18-59 років. Вони отримали вакцину CoronaVac. Результати клінічного випробування показали, що вакцина нейтралізує антитіла через 14 днів після вакцинації за графіком 0,14 дня.
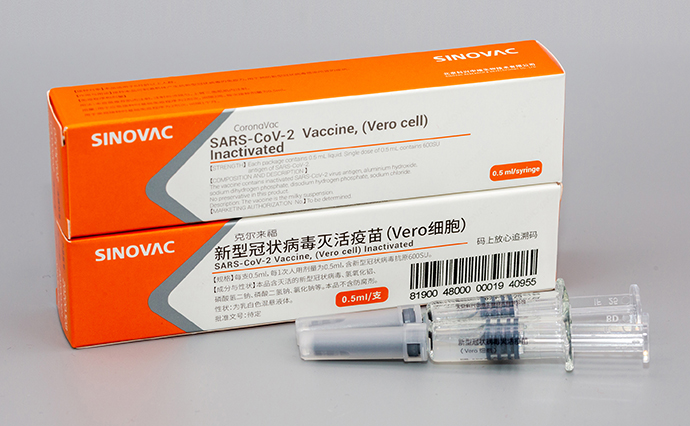
Китайська інактивована вакцина CoronaVac
ДЖЕРЕЛО: SINOVAC.COM
7 липня компанія повідомила про старт третьої фази клінічних випробувань. Випробування пройде в Бразилії, де місцевий регулятор видав відповідний дозвіл. У дослідженні візьмуть участь 9 тис медичних працівників.
У Sinovac сподіваються, що вакцина буде готова у 2020 році. Компанія здатна виробляти 100 млн одиниць на рік.
Акції Sinovac торгуються на Nasdaq. Її продуктовий асортимент включає вакцини проти ентеровірусу, гепатиту А і В, сезонного грипу, пташиного і свинячого грипу, варицели та паротиту. У 2009 році Sinovac стала першою компанією світу, яка отримала схвалення щодо вакцини проти грипу H1N1.
2. University of Oxford, AstraZeneca
Дослідники Оксфордського університету спільно з британською фармацевтичною компанією AstraZeneca розробили вакцину AZD1222.
Виступаючи 1 липня на парламентських слуханнях, професор вакцинології Оксфордського університету Сара Гілберт заявила, що 8 тис добровольців було зараховано на третю фазу випробування вакцини. "Ми бачимо правильний тип імунної відповіді, який забезпечить захист", - сказав Гілберт.
Хоча клінічні випробування вакцини ще тривають, AstraZeneca вже укладає угоди з урядами європейських країн на поставку сотень мільйонів доз вакцини. Зокрема, вона домовилася з Європейським альянсом інклюзивних вакцин (IVA) про постачання до 400 млн доз вакцини від COVID-19.
11 липня міністр охорони здоров'я України Максим Степанов заявив, що Україна хоче отримати вакцину AstraZeneca однією з перших.
"Я звернувся до своїх колег, міністрів охорони здоров'я Німеччини, Франції, Італії та Нідерландів, щоб у разі виготовлення вакцини Україна також отримала цей препарат. Я хочу, щоб наша країна була в пріоритеті", - сказав Степанов.
В AstraZeneca кажуть, що першу партію, 15,2 млн доз, вироблять до грудня 2020 року, другу - у січні 2021 року. Це буде зроблено до реєстрації препарату.
Між тим, виконавчий секретар Міністерства охорони здоров'я Бразилії Ельчіо Франко заявив, що уряд країни придбає в AstraZeneca за 127 млн дол технологію і матеріали для виробництва вакцини AZD1222. Якщо вона виявиться ефективною, бразильцям будуть доступні 100 млн доз.
AstraZeneca - англо-шведська фармацевтична компанія з річним оборотом 30 млрд дол, акції якої торгуються на Нью-Йоркській фондовій біржі. Фірма розробляє, продукує і продає препарати, що застосовують в гастроентерології, кардіології, судинній патології, неврології, психіатрії, пульмонології, онкології.
У травні 2020 року компанія отримала 1 млрд дол від Управління перспективних біомедичних досліджень і розробок (BARDA) Міністерства охорони здоров'я США на випуск вакцини від коронавірусу COVID-19.
3. CanSino Biological Inc., Beijing Institute of Biotechnology
Недавно завершилася друга фаза клінічних випробувань вакцини Ad5-nCoV, створеної китайською компанією CanSino Biologics та Пекінським інститутом біотехнології в Академії військово-медичних наук.
Як і вакцина з Оксфорда, тут використовується ослаблений аденовірус. За підсумками другої фази вакцина була схвалена для використання серед китайських військових. Її також затвердили для клінічних випробувань у Канаді.
На фазі першого клінічного випробування серед 107 здорових людей вакцина змогла генерувати відповідь на антитіла після 28 днів вакцинації.
Волонтери отримали одну ін'єкцію вакцини Ad5 з трьома різними дозами: високою, середньою та низькою. Потім дослідники регулярно тестували зразки крові учасників, щоб оцінити, чи активувала вакцина дві частини імунної системи організму: "гуморальну відповідь" та реакцію Т-клітин.
Усі дози вакцини спричинили певний рівень імунної відповіді протягом двох тижнів. Одне з обмежень вакцини полягає в тому, що вона не працює добре в людей, у яких вироблений високий імунітет до аденовірусу.
Акції CanSino торгуються на біржі Гонконгу. Компанія досліджує та виробляє вакцинні препарати для людей. Основні продукти - менінгококові вакцини MCV4 та MCV2. Компанія в основному працює на внутрішньому ринку Китаю.
4. Moderna, NIAID
Великі сподівання у справі розробки вакцини від COVID-19 світ покладає на американську компанію Moderna. Кілька днів тому вона оголосила про початок третьої фази клінічних випробувань вакцини mRNA-1273.
Плацебо-контрольоване дослідження включатиме 30 тис учасників, доза становитиме 100 мкг. Компанія завершила виробництво вакцини для початку дослідження третьої фази. Вона готується виробляти 500 млн доз вакцини на рік і, можливо, 1 млрд доз на рік з 2021 року. Виробництво розташують у США.
Днями стало відомо, що Moderna та іспанська фармакологічна компанія Laboratorios Farmacéuticos Rovi, SA, що спеціалізується на контрактному виробництві біологічних продуктів і малих молекул, оголосили про співпрацю.
Відповідно до угоди, вакцина мРНК-1273 буде вироблятися на підприємстві ROVI в Мадриді і потрапить на міжнародний ринок на початку 2021 року.
Компанія Moderna фокусується на дослідженнях у сфері mRNA. Ця біотехнологія дозволяє створити новий клас ефективних лікарських засобів. Вони "примушують" клітини виробляти білки, які можуть мати терапевтичну або профілактичну користь і мають потенціал боротьби з низкою захворювань.
У травні 2020 року вартість компанії Moderna була оцінена 30 млрд дол.
5. Inovio Pharmaceuticals, International Vaccine Institute
Американська компанія Inovio розробляє ДНК-вакцину INO-4800 і в липні, після отримання відповідного дозволу, планує почати другу і третю фази тестування.
За даними компанії, 94% учасників першої фази клінічних випробувань продемонстрували загальну імунну відповідь на шостому тижні після двох доз вакцини. На цьому етапі в досліджені брали участь 40 здорових добровольців.
У доклінічному дослідженні на тваринах INO-4800 забезпечив повний захист від реплікації SARS-CoV-2 у легенях мишей, заражених вірусом.
Цікаво, що компанія розробила дизайн вакцини протягом трьох годин після отримання результатів розшифровування геному вірусу. Це відбулося 10 січня.
Через два тижні Inovio отримала грант на 9 млн дол від фонду "Коаліція за інновації в забезпеченні готовності до епідемій". У березні вона отримала грант на 5 млн дол від Біла та Мелінди Гейтс і грант на 11,9 млн дол від Міноборони США. Ще 71 млн дол Inovio отримала від Міноборони США в червні на розробку і виробництво смарт-пристрою для доставки вакцини в шкіру.
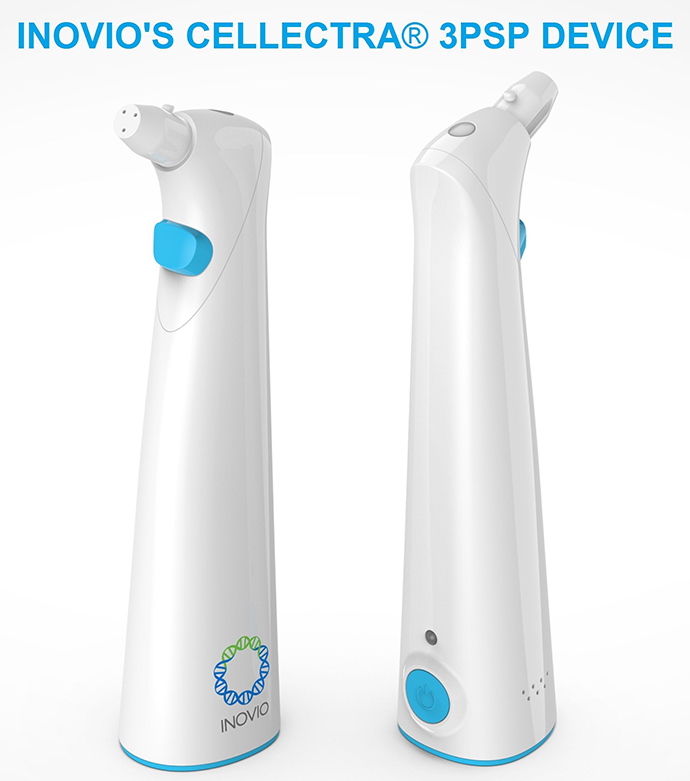
Смарт-пристрій CELLECTRA 3PSP для доставки вакцини INO-4800 в шкіру
ДЖЕРЕЛО: PRNEWSWIRE.COM
Швидкість, з якою була розроблена вакцина INO-4800, в Inovio пояснюють перевагою платформи ДНК, на основі якої створюються лікарські засоби.
"Переваги платформи ДНК-ліків у тому, що такі препарати можна швидко розробляти і виготовляти. Ці препарати стійкі і не потребують зберігання й транспортування в замороженому вигляді. Вони забезпечують міцну імунну реакцію та сприятливий профіль безпеки", - кажуть у компанії.
Вакцина INO-4800 вводить в організм людини частину генетичного коду вірусу, у результаті чого клітини починають виробляти антигени - молекулу, присутню на зовнішній поверхні вірусу. У клінічних випробуваннях взяли участь 2 тис людей. Строки початку масового виробництва вакцини поки невідомі.
Inovio називає себе першою і єдиною компанією, яка клінічно продемонструвала введення лікарського засобу на ДНК-платформі безпосередньо в клітини організму. Зокрема, мова йде про протиракову вакцину VGX-3100, яка перебуває на третій фазі клінічних випробувань.
У підсумку
Поки сотні компаній розробляють вакцини проти COVID-19, а уряди готують сотні мільйонів доларів на їх закупівлю, провідний експерт з інфекційних недуг США Ентоні Фочі застерігає: майбутня вакцина проти коронавірусу не буде такою ж ефективною, як вакцина проти кору, яка захищає людину все життя.
"Ми отримаємо захист на певний час, принаймні, щоб пройти через цей цикл пандемії. У майбутньому нам доведеться посилювати засоби", - каже він.







